Mesure de concentration dans les liquides
Principes de la mesure de concentration
La détermination de la concentration de différents liquides joue un rôle crucial dans de nombreux procédés divers. Elle consiste à mesurer et évaluer le rapport entre deux substances dans un mélange ou une solution.
Un facteur central de cette mesure de concentration est la concentration en quantité de matière. Elle est définie comme la quantité d'une substance par unité de volume et est particulièrement cruciale dans l'analyse des solutions. Elle permet une évaluation précise de la composition chimique et de la réactivité, devenant ainsi un outil indispensable dans de nombreux domaines.
De plus, il existe différentes plages de mesure qui permettent de mesurer la concentration en quantité de matière de diverses manières. Elles élargissent considérablement les possibilités de mesure de concentration et augmentent la flexibilité par rapport aux exigences spécifiques du mélange ou de la solution à analyser.
Enfin, la quantité de liquide à analyser joue un rôle important. Elle doit être suffisante pour permettre une mesure précise, mais pas trop grande pour ne pas fausser le résultat ou compliquer inutilement la mesure.
Un aspect important de la mesure de concentration est la concentration en quantité de matière (molarité) dans une solution, définie comme la quantité d'une substance par unité de volume. Ceci est particulièrement pertinent lors de l'analyse d'une solution, où la concentration en quantité de matière est cruciale pour évaluer la composition chimique, les concentrations et la réactivité. La mesure précise des concentrations d'une quantité de matière dans une solution est essentielle pour contrôler les processus, garantir la qualité et mener des études scientifiques.mener des études.
La méthode de mesure par ultrasons de LiquiSonic®
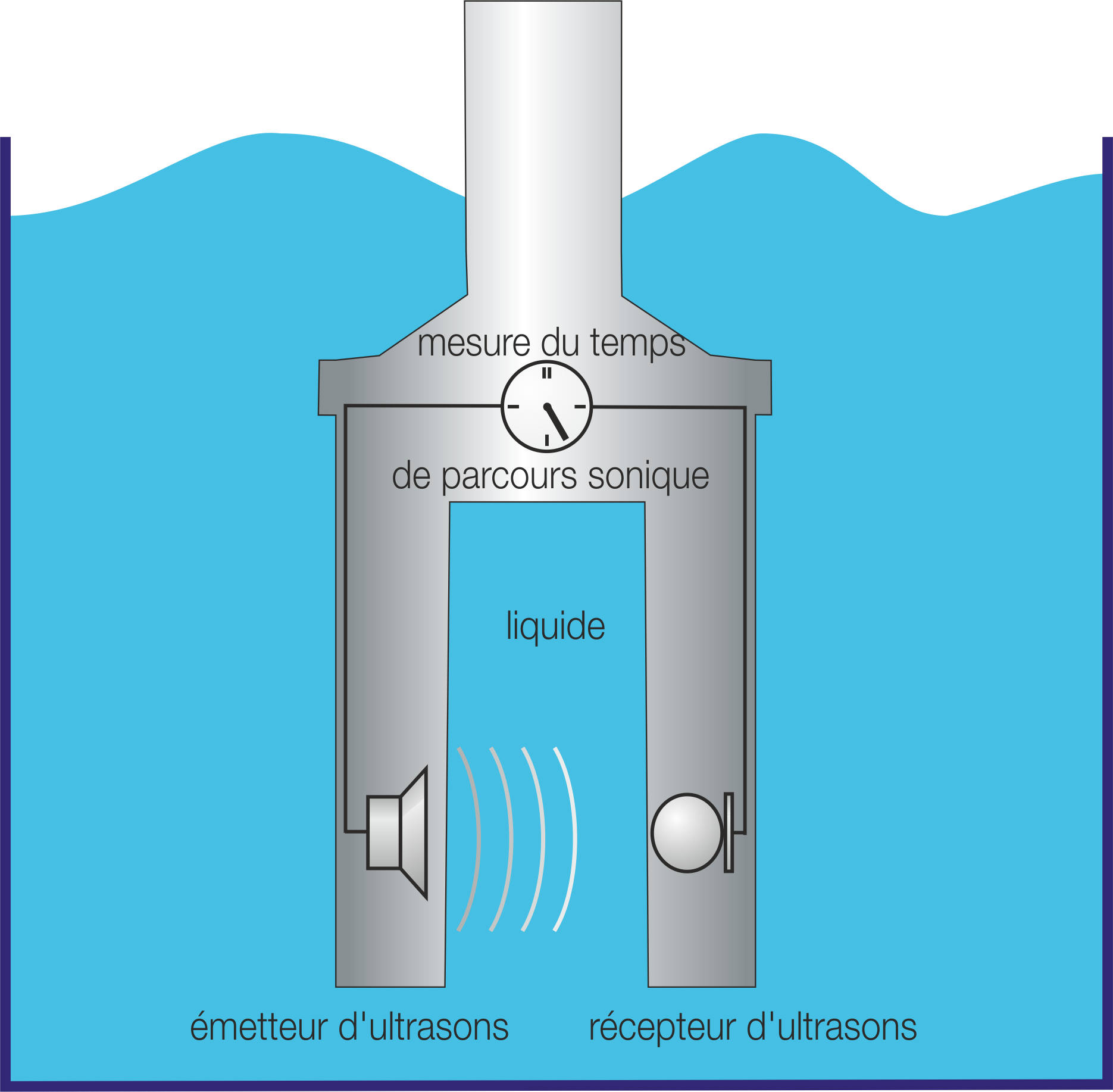
Le principe de la méthode de mesure est une mesure du temps qui peut être réalisée avec une grande précision et stabilité à long terme. La concentration ou la densité d'un liquide est calculée à partir de la vitesse du son. D'autres paramètres peuvent également être déterminés, tels que le contenu en Brix, la teneur en solides, la matière sèche ou la densité de suspension.
Nos LiquiSonic® Appareils de mesure de concentration et de densité sont utilisés dans divers processus pour l'analyse des liquides.
Dans le cas typique, une courbe d'étalonnage est déterminée à partir de la relation entre la vitesse du son et la concentration. Sur cette base, la concentration correspondante est calculée à partir de chaque valeur de vitesse du son mesurée.
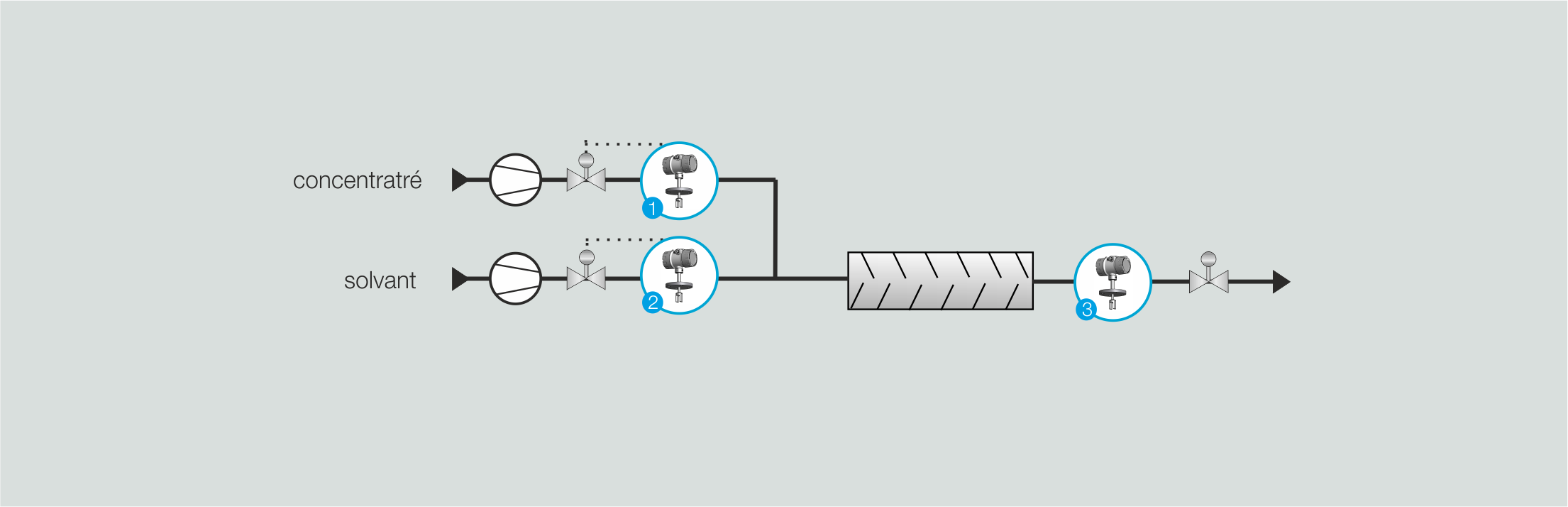
Réglage de la concentration
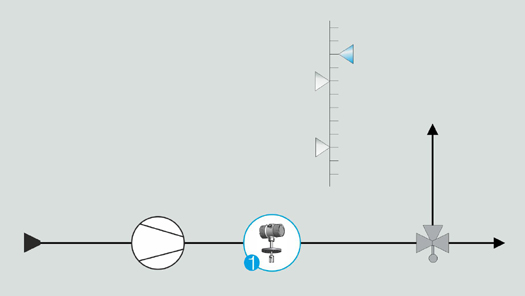
Surveillance des valeurs limites
Nos appareils de mesure par ultrasons n'ont pas de pièces mécaniques susceptibles de s'user ou de vieillir. Ils présentent des avantages exceptionnels par rapport aux méthodes de mesure concurrentes pour déterminer la concentration et la densité.
Haute fiabilité dans la détermination de la concentration en quantité de matière
La méthode de mesure nécessite seulement une mesure précise du temps pour déterminer la concentration en quantité de matière. La vitesse du son est calculée à partir du temps de parcours du son et de la distance connue entre l'émetteur et le récepteur. La construction typique du capteur comprend l'émetteur et le récepteur dans un boîtier compact.
La méthode de mesure est indépendante de la conductivité, de la couleur et de la transparence du liquide grâce aux capteurs, et se distingue par une haute fiabilité dans la détermination de la concentration en quantité de matière. La précision de mesure des appareils se situe entre 0,05 m% et 0,1 m%. En plus de la mesure de la vitesse du son, tous LiquiSonic® Capteurs disposent d'une mesure intégrée de la température pour la compensation de température dans le processus.
Applications des mesures de concentration
La mesure de la concentration est l'une des méthodes essentielles pour analyser la qualité et les caractéristiques de sécurité des produits et des substances. Elle joue donc un rôle crucial dans plusieurs industries. Il existe différentes méthodes pour mesurer la concentration en quantité de matière dans une solution, en fonction du type de substance et des exigences de l'application.
Un exemple pratique de l'application de la mesure de concentration se trouve dans l'industrie pharmaceutique : ici, la détermination précise de la concentration d'un principe actif dans les médicaments est essentielle pour garantir leur efficacité et leur sécurité. Cela montre l'importance des méthodes de mesure précises pour déterminer une concentration de la quantité de substance dans le contrôle qualité.
D'autres exemples :
- Chimie/ Production chimique (Pour surveiller la composition des mélanges)
- Production alimentaire (Pour contrôler la qualité des produits alimentaires)
- Métallurgie (Pour vérifier la qualité des minerais métalliques)
- Analyse environnementale (Pour calculer les polluants dans l'eau)
De plus, la mesure de concentration est également utilisée dans de nombreux autres domaines, par exemple dans la science.